FDA 510K注册
所谓的FDA510K,就是美国食品、药品和化妆品(FD&C)行动委员会的一个法案章节,而这个法案的章节,正好是在美国FD&C Act第510章节,所以很多人习惯性的把他称作是510K,而且这个是美国食品、药品和化妆品(FD&C)行动委员会法案,所以大家又都喜欢叫它做FDA510K,这就是所谓的FDA510K的由来。

根据这个 510K 章节的法案要求,凡是把法规规定的器械引入美国市场时,都必须满足该法案的要求,那些不豁免 510K 的 I、II、III 类医疗器械,都必须做“产品上市登记”,这个产品上市登记,就是我们通常所说的 FDA 510K 注册。
为什么要进行FDA 510K 注册
生产企业须在产品上市前通过 FDA 510K 审查,产品才能够在美上市销售。而且做 FDA 510K 注册有下列好处:
1.一次性费用,后续无任何费用
2.公司做任何变化,K 号不变,属于公司永久的无形固定资产
3.公司上市或被收购时,通常至少按 10 倍的价格做固定资产来估价
4.获得批准后续无需做任何工作,永久持有
哪些产品需要FDA 510K注册
根据风险等级的不同,FDA 将医疗器械分为三类(I、II、III),III 类风险等级最高,I 类风险等级最低。
I 类中极少数保留产品需要做 FDA 510K 注册。
II 类产品大多数均需要做 FDA 510K 注册。
III 类产品绝大部分都需要做上市前许可而不是 FDA 510K 注册。
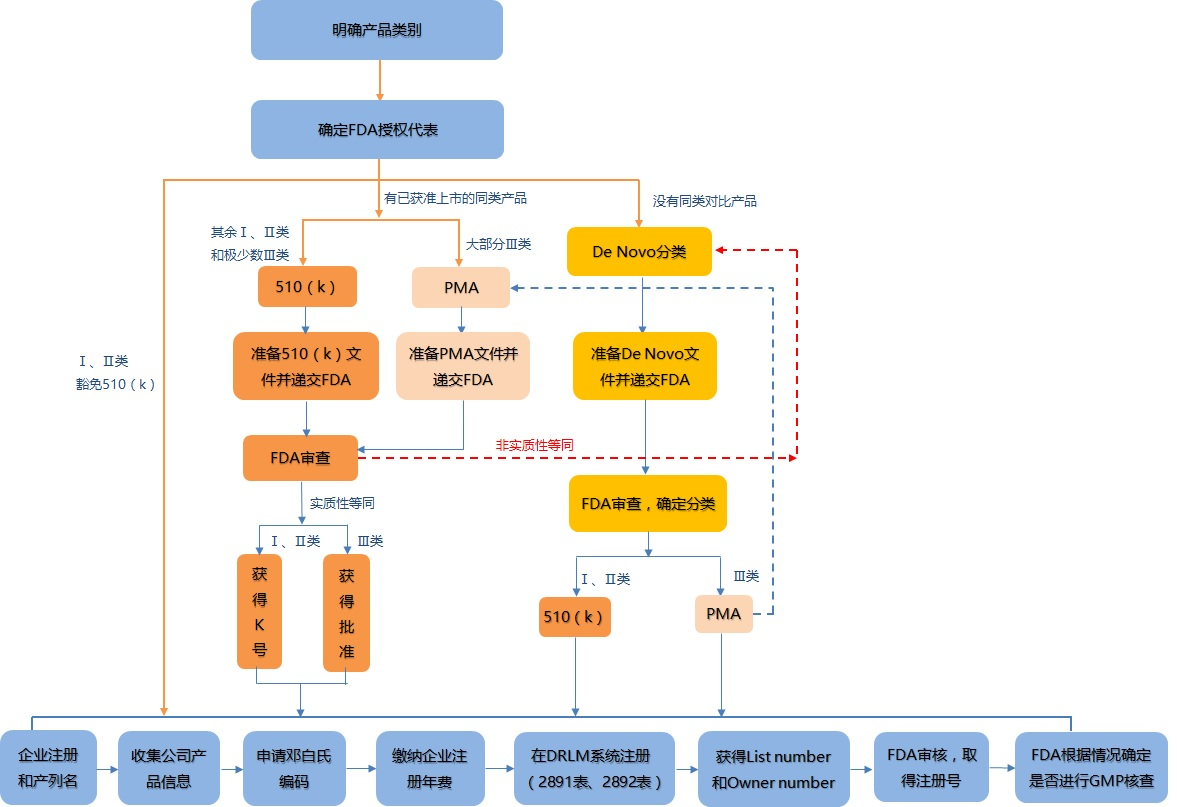
FDA 510K注册流程
世界范围内的医疗器械的入市标准向来严格。考虑到美国医疗器械技术水平与市场成熟度较高,其监管力度与其行业技术发展水平相得益彰,FDA根据医疗器械的分类标准及是否存在实质等同产品采取并行的多种类入市标准。中国医疗器械生产企业需要按照分类标准,严格执行申请程序才能够实现自身产品在美国市场上市销售。